![]() Los medios de comunicación franceses informaban a finales de 2012 de cuatro muertes en ese país relacionadas con el empleo de ciproterona en combinación con etinilestradiol y de la denuncia —presentada por una mujer tratada con un anticonceptivo hormonal combinado de tercera generación que sufrió un accidente cerebrovascular— contra la Agencia Nacional de Seguridad de los Medicamentos (ANSM) y la compañía Bayer. Unas semanas antes, en noviembre de ese año, la Haute Autorité de Santé (HAS) había alertado del mejor perfil de seguridad de los anticonceptivos hormonales combinados de primera y segunda generación respecto a los más nuevos, en relación al riesgo de sufrir un tromboembolismo venoso, la principal reacción adversa de estos medicamentos.
Los medios de comunicación franceses informaban a finales de 2012 de cuatro muertes en ese país relacionadas con el empleo de ciproterona en combinación con etinilestradiol y de la denuncia —presentada por una mujer tratada con un anticonceptivo hormonal combinado de tercera generación que sufrió un accidente cerebrovascular— contra la Agencia Nacional de Seguridad de los Medicamentos (ANSM) y la compañía Bayer. Unas semanas antes, en noviembre de ese año, la Haute Autorité de Santé (HAS) había alertado del mejor perfil de seguridad de los anticonceptivos hormonales combinados de primera y segunda generación respecto a los más nuevos, en relación al riesgo de sufrir un tromboembolismo venoso, la principal reacción adversa de estos medicamentos.
El revuelo mediático generado motivó que Francia instara a la Agencia Europea del Medicamento (EMA) a revisar la seguridad de estos fármacos en el seno del recién creado Comité para la Evaluación de Riesgos en Farmacovigilancia (PRAC). Además, las autoridades sanitarias francesas decidieron desfinanciar los anticonceptivos de tercera y cuarta generación y retirar del mercado durante tres meses aquellos medicamentos que contuviesen ciproterona en su composición, a la espera de la decisión final de las autoridades europeas.
No obstante, el debate sobre el mayor riesgo tromboembólico de los anticonceptivos combinados de las últimas generaciones no era nuevo y las distintas agencias reguladoras ya lo habían abordado anteriormente. En 2001, la EMA revisó la seguridad de los de tercera generación (con desogestrel o gestodeno como progestágeno), advirtiendo a los profesionales sanitarios del mayor riesgo tromboembólico en comparación con los de segunda generación (con levornorgestrel como progestágeno). En 2011, la Food and Drug Administration (FDA) tuvo que pronunciarse sobre la seguridad tromboembólica comparada de los anticonceptivos que contienen drospirenona (cuarta generación) debido a la publicación de dos estudios observacionales, realizados de forma retrospectiva con dos registros de datos clínicos, en los que se evidenció un incremento del riesgo tromboembólico en las mujeres tratadas con drospirenona. Estos resultados ya se habían observado en estudios previos. El tibio comunicado emitido en ese momento por la FDA estuvo acompañado de la polémica por los conflictos de interés de algunos de los miembros del panel encargado de la revisión. La Medicines and Healthcare Products Regulatory Agency (MHRA) británica también informó en ese momento de los resultados de los dos estudios y alertó del mayor riesgo tromboembólico de la drospirenona y de la necesidad de seleccionar el anticonceptivo más apropiado en función del riesgo basal de cada mujer.
Durante todo ese tiempo, en nuestro país no se emitió ninguna recomendación orientada a restringir la prescripción de los anticonceptivos de tercera y cuarta generación, en relación con los nuevos datos que se iban conociendo, y únicamente se modificó la información de la ficha técnica y el prospecto, lo que se informó en este y este informes mensuales de la AEMPS. Es más, los anticonceptivos con drospirenona pasaron a estar financiados por el Sistema Nacional de Salud poco después de conocerse los dos estudios observacionales mencionados anteriormente, como consecuencia de la publicación de la “Ley Orgánica 2/2010 de salud sexual, reproductiva y de interrupción voluntaria del embarazo”, sin que se hiciera público ningún informe técnico a propósito de las diferencias de riesgo tromboembólico entre este progestágeno y el resto.
En febrero de 2013, después de la solicitud del estado francés, la EMA anunciaba el inicio de la revisión de la seguridad de los anticonceptivos combinados de tercera y cuarta generación y en mayo modificaba las condiciones de utilización de las combinaciones de ciproterona, incidiendo en la contraindicación de emplearlas como anticonceptivo.
Durante el transcurso de esa evaluación europea, en julio de 2013, el Ministerio de Sanidad anuncia que deja fuera de la financiación del Sistema Nacional de Salud a los compuestos que incluyen drospirenona. En seguida aparecen las voces críticas que sitúan esta decisión dentro de la política de recortes sanitarios que se producen en ese momento y hay quien opina que prescindir de esta combinación anticonceptiva es “como volver a los ochenta”. Y aunque muchos profesionales defendieron la medida, lo cierto es que no se adoptó buscando mejorar la seguridad en el uso de los medicamentos por parte de los ciudadanos, sino que respondió a una discrepancia entre el Ministerio y las empresas farmacéuticas en el precio de comercialización de estos medicamentos.
Por fin, en octubre de 2013 se conoce el resultado de la evaluación del PRAC, que confirma que los beneficios de todos los anticonceptivos hormonales combinados superan sus riesgos. Este dictamen se traslada al Comité de Medicamentos de Uso Humano de la EMA (CHMP) que, en noviembre, se pronuncia en el mismo sentido que el PRAC y ya en enero de 2014, la EMA establece que se actualice la información dirigida al paciente para ayudar a que las mujeres puedan decidir en relación con la selección del anticonceptivos más apropiado en cada caso.
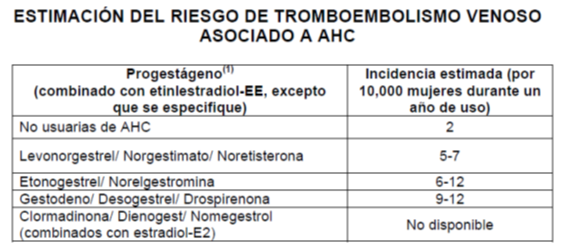
Aunque finalmente la EMA dictamina que el balance beneficio/riesgo de todos los anticonceptivos hormonales combinados es favorable, también deja claro que existen diferencias en cuanto al riesgo de tromboembolismo venoso en función del progestágeno incluido en la composición, tal y como se aprecia en la siguiente tabla, extraída de la nota informativa de la AEMPS:
Las diferencias de riesgo pueden parecer pequeñas, pero el impacto poblacional es muy grande, puesto que hablamos de medicamentos de amplio uso. Así, si asumimos que en nuestro país hay 3 millones de usuarias de este método anticonceptivo, estaríamos hablando de una incidencia anual de eventos tromboembólicos venosos de 1.500-2.100 mujeres afectadas en caso de emplear sólo levonorgestrel como progestágeno frente a 2.700-3.600 mujeres afectadas en caso de utilizar únicamente drospirenona.
Se echa en falta que las autoridades sanitarias españolas pongan en marcha iniciativas encaminadas a promover el uso de los anticonceptivos más seguros. A pesar de que los compuestos de drospirenona se han retirado de la financiación, en los últimos meses se han comercializado genéricos a un precio similar al que tendría la combinación de drospirenona de marca en caso de que se le aplicase una aportación del usuario de un 40%, lo que puede estar provocando que muchas mujeres se estén decantando por esta opción. Por otra parte, las combinaciones con desogestrel (de tercera generación), nunca fueron retiradas de la financiación y siguen financiadas a cargo del Sistema Nacional de Salud. En todo caso, e independientemente de que estén o no financiados, al precisar receta para su dispensación resulta fundamental que los médicos realicen la selección de anticonceptivos de forma informada y responsable.
A diferencia de otros países, en España las decisiones sobre la financiación pública de los anticonceptivos hormonales combinados no parece que estuvieran fundamentadas en criterios científicos. Además, tomando como ejemplo el Reino Unido, debería incrementarse la transparencia del proceso. En el caso de los anticonceptivos, da la impresión de que en nuestro país las decisiones de financiación se adoptaron según la coyuntura político-económica-comercial del momento. Tampoco se ha invertido en campañas de educación sanitaria dirigidas a la población, sobre éste ni sobre otros temas de interés. Ante esta situación, adquiere especial relevancia el papel de los profesionales sanitarios al informar a las mujeres sobre las ventajas y riesgos de los distintos medicamentos anticonceptivos, orientándolas hacia la mejor decisión posible.
[slideshare id=28716716&style=border:1px solid #CCC; border-width:1px 1px 0; margin-bottom:5px; max-width: 100%;&sc=no]
Entrada elaborada por Cecilia Calvo Pita